|
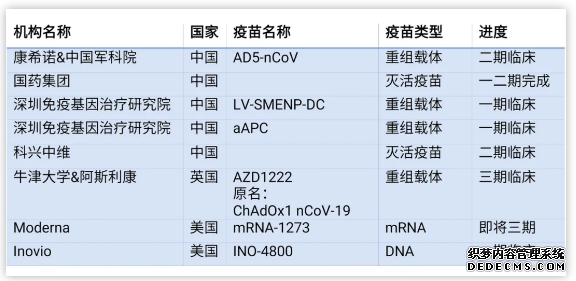
原标题:【动态】智飞生物新冠疫苗获临床批件 来源:医谷 医谷微信号:yigoonet 今日(6月23日),智飞生物发布公告称,其全资子公司智飞龙科马与中国科学院微生物研究所联合研发的重组新型冠状病毒疫苗(CHO 细胞)正式获得国家药监局临床试验申请受理通知书及临床试验批件(批件号:2020L00023、2020L00024),同意进行临床试验,批件有效期为12个月。 据悉,这也是我国首个获批进入临床试验的重组亚单位新冠疫苗。 该重组亚单位新冠疫苗,采用重组DNA技术,以新型冠状病毒刺突糖蛋白(S蛋白)的受体结合区(RBD)作为抗原,再辅以传统佐剂研制而成,其在转基因鼠的攻毒实验中证明了疫苗具有明显的保护效果。恒河猴攻毒保护试验结果显示,疫苗免疫能诱导产生高水平的中和抗体,显着降低肺组织病毒载量,减轻病毒感染引起的肺部损伤,具有明显的保护作用。同时,该疫苗通过工程化细胞株进行工业化生产,产能高,成本低,具有较强的可及性。 根据智飞生物公告,疫苗将随后将进入人体临床试验阶段,Ⅰ期临床试验将分别在重庆医科大学附属第二医院和首都医科大学北京朝阳医院开展。 据了解,按现有产能计算,一旦获批,智飞龙科马的重组亚单位新冠疫苗年产能可达3亿剂、1.5亿人份。 此外,据科技部6月19日的发布数据,目前中国已有1个腺病毒载体疫苗和4个灭活疫苗正式获得国家药监局批准开展临床试验,国外,Moderna、牛津大学、Inovio的疫苗也都在临床试验中,其中Moderna近日宣布,该公司计划在7月份对mRNA-1273进行3万名志愿者的最终测试。
文| 医谷
海量资讯、精准解读,尽在新浪财经APP |